科兴疫苗(图片来源:Getty Images)
【看中国2021年6月10日讯】(看中国记者文俪综合报导)日前,科兴控股生物技术有限公司董事长尹卫东表示,科兴中维未成年人人群的临床研究已经完成一期和二期,称据数百人的临床结果表明,3岁-17岁接种科兴疫苗后安全性良好,现国家已将科兴疫苗紧急使用年龄范围扩大到3岁以上。
据官媒《北京日报》6月5日报导,科兴控股生物技术有限公司董事长尹卫东表示,科兴中维早在今年年初就启动了未成人人群COVID-19灭活疫苗的临床研究,目前已经完成一期和二期临床。据数百人的临床研究结果,3岁-17岁的儿童接种疫苗后,安全性是良好的,和18岁成人组一样安全,且抗体水平也和成年人一样。
尹卫东称,安全有效性的数据已经报到了联防联控机制和国家药监局。目前该公司已提出灭活疫苗的紧急使用申请,并称当局已经批准将科兴灭活疫苗紧急使用年龄范围扩大到3岁以上。更低年龄组具体使用时间将由卫健委专家等推动。
不过,值得注意的是,官方的报导中,并未具体说明参与临床研究的“数百人”到底是几百人,也未公开研究数据。
另外,报导还称,当地时间6月1日,世卫组织宣布将中国科兴灭活疫苗列入“紧急使用清单”。
上述消息一经发布,引发中国网民的关注。大部分网友质疑临床数据不透明,不敢给孩子接种:“数百人?几百?安全性良好?什么叫良好?怎么量化?你们家研究科学,研究疫苗就这么不严谨?让谁信服呢?”、“这次我真的不支持对儿童紧急开放,数据真的不齐全就向最小至3岁的儿童开放,确实不太严谨。”
“数百人就可以了吗?对于基数这么大的群体,就几百人,跟踪了多久?三期都还没做,科学不都是严谨的吗?不良率的孩子就该倒霉是吗?为了利益,就可以剥夺人的尊严和平等的权利吗?为了大局就是要牺牲一些人是吗?”
“这并不是个好消息,数百人的实验就能保证安全?三年五年十年后的影响,你们做过实验吗”、“数百人的临床试验后,就能推广给几亿人?一期和二期的临床加起来是几个月?传统疫苗研发时间跨度长达多年,新冠疫苗一年就能上市了。之前出事故的长生生物科技公司给孩子打的疫苗,也是经过批准的(上次看央视新闻,日本宫颈癌疫苗的副作用,有的两年后才凸现)。
“太可怕了,这么短时间的临床,就要全面铺开、没有大量实际数据做支撑,不敢打。”
网友质疑,这种新闻究竟要传递什么信息?要不就是国家卫健委发布消息,要不就把您做的研究发表出来!你一个董事长出来表示啥?一个商业公司的代表。打疫苗没问题,信息公开透明是关键。
还有网友担心会强制接种,如不让接种不准进学校,最后非得逼的小孩子都接种:“一直以来都是要打疫苗的证,不打不让进小区,不让进学校,咋办?”
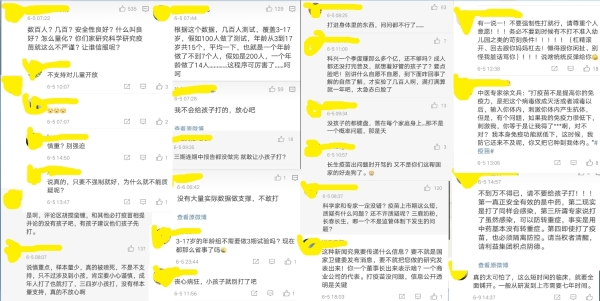
网民担忧儿童接种疫苗(图片来源:微博)
国产疫苗频出问题
虽然中国官方从未报导过任何有关国产疫苗副作用的消息,但还是有受害者透过多种渠道向外界披露接种疫苗后产生严重副作用甚至死亡的案例。
如有网友在推特爆料指,北京三一重工车间一位工人3月21日注射科兴疫苗,23日死亡;微博账户“山下花野子”发文披露自己弟弟今年1月份施打了国药集团的北生灭活疫苗后,产生严重的副作用,于4月15日去世;4月14日,希望之声接到国内民众爆料,2021年3月末左右,辽宁省大连庄河市桂云花乡岭西村村民王大军,男,43岁,接种疫苗后,当天死亡;
5月底,西安90后女孩“田一千”在微博发文披露自己接种科兴疫苗第一针后产生严重副作用,心脏衰竭。医生称她有冠心病,至6月2日,“田一千”未在微博更新消息,而其去向也成谜。推特上有消息传该女已经去世,但相关消息尚无法得到证实。官方也未见报导。
6月1日,“背对背说不见”的微博用户发文,披露自己弟弟在接种国产(北京生物)COVID-19疫苗后,出现严重副作用,至今已在重症监护室20多天。最近一次更新微博是6月7日,之后再无消息。
另外,截止今年4月21日,香港累计25人接种疫苗后死亡的事件中,有21人曾施打科兴疫苗、4人接种上海复星医药和德国BioNTech合作生产的“复必泰疫苗”。另在4月5日至18日间发生至少20起接种疫苗后疑似出现面部瘫痪“贝尔氏麻痹症”个案,其中12人曾施打科兴疫苗,8人施打复必泰。
而微博上相关话题下,也总有网友留言表示,自己的亲人接种疫苗后几天便去世,如其中一网友表示:“虽然不知道是不是因为疫苗,但是我爸爸确实打完没两天就突发心梗死了,我觉得或多或少有一些关系吧。”
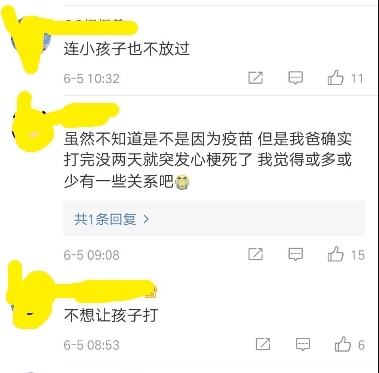
有网友表示自己父亲接种国产疫苗后突发心梗离世(图片来源:微博)
来源:看中国
短网址: 版权所有,任何形式转载需本站授权许可。 严禁建立镜像网站.
【诚征荣誉会员】溪流能够汇成大海,小善可以成就大爱。我们向全球华人诚意征集万名荣誉会员:每位荣誉会员每年只需支付一份订阅费用,成为《看中国》网站的荣誉会员,就可以助力我们突破审查与封锁,向至少10000位中国大陆同胞奉上独立真实的关键资讯,在危难时刻向他们发出预警,救他们于大瘟疫与其它社会危难之中。










